摘要:GALLIUM 研究显示,在未经治疗的滤泡性淋巴瘤和边缘区淋巴瘤患者中,奥妥珠单抗基于的免疫化疗方案在无进展生存期上显著优于利妥昔单抗方案,还能延长患者开启下一次抗淋巴瘤治疗的时间;两者总体生存率相近,安全性相当。奥妥珠单抗常见副作用包括输液反应、感染、血液系统异常等,严重时可引发肿瘤溶解综合征,它已成为一线治疗高级别滤泡性淋巴瘤的标准方案 。
在非霍奇金淋巴瘤(NHL)治疗领域,新型药物的研发与应用始终是改善患者预后的关键。奥妥珠单抗作为一款备受瞩目的单克隆抗体药物,在未经治疗的惰性非霍奇金淋巴瘤(iNHL)患者治疗中逐渐崭露头角。其中,GALLIUM 研究以严谨的设计和详实的数据,为奥妥珠单抗的临床价值提供了强有力的证据支撑。
GALLIUM 研究:对比验证奥妥珠单抗实力
GALLIUM 研究是一项关键的 III 期临床试验,其核心目标在于对比奥妥珠单抗与传统利妥昔单抗,在治疗初治滤泡性淋巴瘤(FL)和边缘区淋巴瘤(MZL)患者时的安全性与有效性。该研究广纳 1202 名 FL 患者,通过 1:1 随机分组的方式,使患者分别接受基于奥妥珠单抗或利妥昔单抗的免疫化疗方案,并进行最长达 2 年的维持治疗,严谨的实验设计为结果的可靠性奠定基础。
显著疗效:无进展生存期显著延长
最终研究分析结果令人振奋,在无进展生存期(PFS)这一重要指标上,奥妥珠单抗基于的免疫化疗方案优势显著。经过长达 7.9 年的中位随访,奥妥珠单抗组 7 年 PFS 率高达 63.4%,而利妥昔单抗组为 55.7%(P = 0.006)。同时,在开始下一次抗淋巴瘤治疗的时间维度,奥妥珠单抗组同样表现出色,7 年内无需开启下一次治疗的患者占比为 74.1%,高于利妥昔单抗组的 65.4%(P = 0.001),这意味着患者能够在更长时间内维持病情稳定,减少后续治疗带来的负担。
生存与安全:整体生存与安全性表现
然而,在总体生存率(OS)方面,两组数据呈现相似态势,奥妥珠单抗组为 88.5%,利妥昔单抗组为 87.2%(P = 0.36),这暗示奥妥珠单抗在延长无进展生存期上虽表现优异,但对总体生存率的影响还需更多研究探索。
在安全性评估上,奥妥珠单抗组严重不良事件发生率为 48.9%,利妥昔单抗组为 43.4%,致死性不良事件发生率在两组间几乎持平(4.4% 与 4.5%) ,且未发现新的安全隐患,证实奥妥珠单抗安全性与利妥昔单抗相当。不过,患者仍需警惕常见副作用,如输液引发的低血压、皮疹、寒战,各类感染风险,血液系统的中性粒细胞减少、血小板减少,以及乙型肝炎病毒再激活、肿瘤溶解综合征等严重情况。
GALLIUM 研究成果为临床治疗带来新方向,奥妥珠单抗已成为一线治疗高级别 FL 的标准方案,能为患者带来长期临床获益。随着临床应用的推进与研究的深入,基于患者个体差异优化奥妥珠单抗的使用策略,探索其在更多淋巴瘤亚型治疗中的潜力,将成为未来的重要研究方向,有望为淋巴瘤患者带来更多治疗希望。
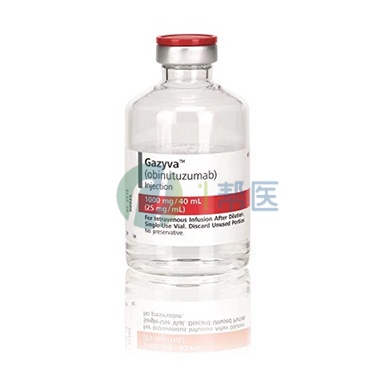
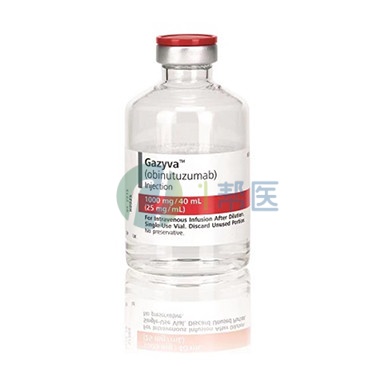
 奥滨尤妥珠单抗(Obinutuzumab)
奥滨尤妥珠单抗(Obinutuzumab) 注射剂
1000mg/40mL
 瑞士罗氏
瑞士罗氏
GAZYVA(obinutuzumab)是一种CD20指导的细胞溶解抗体,表示:(1)与苯丁酸氮芥组合,用于治疗以前未经治疗的慢性淋巴细胞白血病患者。
2025-06-03 16:49:19
2025-06-03 16:39:11
2025-06-03 16:31:34
2025-06-03 16:21:52
2022-05-27 16:35:24
2022-05-27 16:45:25
2022-05-30 16:41:11
2022-07-12 16:24:27
2026-03-17 22:26:02
2026-03-17 22:06:52